화학
자연 과학의 한 분야. 물질의 조성과 구조, 성질 및 변화, 제법, 응용 따위를 연구한다. 무기 화학, 유기 화학, 생물 화학, 물리 화학, 분석 화학, 이론 화학, 응용 화학 따위의 갈래가 있다.
- 국립국어원 표준국어대사전
- 목차 -
화학에도 혁명이 있었다! 화학의 역사 ① 물질은 무엇으로 이루어져 있을까?
Comment.
•
짧은 분량 안에서 역사를 다룬다는 것은 많은 것을 생략한다는 말입니다. 언제나 그랬지만 학문 분야의 역사는 더더욱 저의 임의적인 생략이 많을 수밖에 없는데요. 그럼에도 분량이 너무 많아져서 조금씩 나누어서, 격주가 아닌 매주 화학의 역사로 찾아올 예정입니다.
•
지난 번에 다루었던 과학철학의 역사에서 토마스 쿤의 패러다임론이 기억나시나요? 쿤이 패러다임론의 예시로 천동설이 지동설로 변화하는 천문학에서의 혁명뿐만 아니라, 화학 혁명을 이야기합니다. 하지만 저 역시 그랬듯이 화학 혁명은 익숙하지 않은 분이 많으실 텐데요. 그래서 화학의 역사를 준비해 보았습니다.
•
보통 화학은 학문적 분류에 따라 무기화학, 유기화학, 물리화학, 분석화학 등으로 나누어 설명하곤 하는데요. 화학사를 볼 때는 다음 질문에 따라 분류하는 것이 이해가 더 쉬울 것으로 판단했습니다.
① 물질은 무엇으로 이루어져 있을까?
② 원소는 어떻게 결합할까? (③ 원소는 어떤 구조로 결합할까?)
④ 원자는 어떻게 생겼을까?
⑤ 새로운 물질을 만들자!
•
물론 이렇게 분류하는 과정에서 많은 부분이 생략되겠지만, 전체적인 화학 역사의 흐름만 이해하시고 자세한 내용은 전문가의 글을 보시는 것을 추천드립니다.
Fig.1 ‘4→3→2’
Figure.1 17세기 화가 아르투스 볼파르트가 그린 4대 원소
화학은 물질의 조성과 구조 그리고 변화를 연구하는 학문입니다. 고대 그리스의 철학자들은 물질이 무엇으로 구성되어 있는지에 대해 다양한 주장을 했는데요. 탈레스Thales of Miletus 는 물, 데모크리토스Democritus 는 원자 등을 주장했죠. 그중 아리스토텔레스Aristotle 가 주장한 4원소설, 즉 모든 물질은 물, 불, 흙, 공기로 이루어져 있다는 주장이 이후 약 2000년간을 지배하게 됩니다. 아리스토텔레스는 4원소의 성분들은 변환될 수 있다고 했는데, 여기에 낚인 연금술사들이 금속으로 금을 만들려는 시도를 수백 년간 하게 되죠.
Figure.2 파라셀수스. 매독 수은 치료를 발명했다
16세기의 연금술사 파라켈수스Paracelsus 는 아리스토텔레스의 4원소설 대신 소금, 유황, 수은으로 이루어져 있다는 3원진설을 주장했습니다. 참고로 파라켈수스의 본명은 테오프라스투스 폰 호엔하임Theophrastus von Hohenheim 으로 호문쿨루스 실험을 하기도 했죠.
Figure.3 판 헬몬트. 2원소설을 주장했지만 최초로 이산화탄소를 발견하기도 했다
17세기의 연금술사인 얀 밥티스타 판 헬몬트Joan Baptista van Helmont 는 4원소설과 3원질설 모두 부정하고 만물은 능동적인 물과 수동적인 공기로 구성되어 있다는 2원소설을 주장합니다. 이를 증명하기 위해 버드나무를 심어 5년간 물만 주었는데요. 5년 후 버드나무는 45.4kg에서 74.4kg으로 늘었고, 흙은 단 57g밖에 줄지 않았죠. (문헌마다 수치가 조금씩 다름) 이를 통해 버드나무는 물과 공기로 이루어져 있다는 결론을 내렸죠.
Figure.4 최초의 화학자 로버트 보일
로버트 보일Robert Boyle 은 1661년 <회의적 화학자>에서 화학과 연금술을 구분하고 아리스토텔레스의 4원소설(불, 물, 흙, 공기)과 파라켈수스의 삼원론(수은, 황, 소금) 등을 부정하고 작은 미립자들이 서로 다른 종류와 개수로 모여 물질을 형성한다는 현대적 원자, 분자에 대한 개념을 제시합니다. 이로써 연금술의 시대가 가고 다양한 분자와 원자들이 등장할 수 있는 토대가 마련됩니다.
Fig.2 뭔가 조금 잘못된 기체 발견의 시대
Figure.5 조지프 프리스틀리의 실험 장비
보일이 스스로를 화학자라고 선언했지만, 아직 연금술사들이 공존하던 시대였습니다. 그중 연금술사 요한 베허Johann Becher 는 1667년 <지하 세계의 물리>에서 흙을 연소성과 광택을 기준 삼아 세 가지로 나누었습니다. 그중 연소성이 있는 흙을 플로지스톤이라고 이름 붙였죠.
베허의 제자였던 게오르크 슈탈Georg Stahl 이 플로지스톤을 체계화합니다. 나무는 딱딱하고 차갑지만 타기 시작하면 그 속에서 뜨거운 불이 계속해서 나오는데요. 슈탈은 나무 속에 플로지스톤이 들어 있었기 때문이라고 보았습니다. 슈탈은 플로지스톤으로 연소 작용뿐만 아니라 금속성, 산성, 알칼리성, 꽃의 색과 향기, 화학적 반응성 및 합성 등을 설명했죠. 이처럼 플로지스톤 이론은 많은 화학 현상을 설명할 수 있었기 때문에 정설로 받아들여졌습니다.
Figure.6 조지프 프리스틀리. 탄산수, 지우개를 최초로 발명하기도 했다
1774년 플로지스톤 이론의 지지자였던 조지프 프리스틀리Joseph Priestley 는 녹이 플로지스톤을 빨아들이면 금속이 되는 실험을 밀폐된 공간에서 시도해 플로지스톤이 결핍된 공기를 얻고자 했습니다. 그렇게 해서 얻어낸 공기를 ‘탈 플로지스톤 공기’(산소)라고 불렀죠.
한편 헨리 캐번디시Henry Cavendish 는 1766년 금속에 산을 녹였을 때 나오는 기체(수소)를 발견합니다. 이 기체를 모아서 불을 붙여보니 펑하고 탔습니다. 캐번디시는 산이 금속을 플로지스톤과 녹으로 분해시킨다고 생각했습니다. 즉, 자신이 발견한 가연성 기체가 플로지스톤 그 자체라고 본 것이죠.
Fig.3 ??? : 그거 아닌데
Figure.7 라부아지에, 세금징수원으로 일한 죄(?)로 프랑스 혁명 시기 단두대에서 처형당했다
하지만 플로지스톤 이론에는 문제가 있었습니다. 목재를 태우면 질량이 감소하는 것은 플로지스톤이 날아가는 것으로 설명할 수 있었지만, 금속은 정반대였습니다. 금속을 태우면 질량이 증가하고, 재(금속회)를 태우면 질량이 감소하죠. 이에 일부 플로지스톤 지지자들은 금속의 플로지스톤이 음의 질량을 가진다고 주장하기도 했고, 플로지스톤이 너무 가벼워서 플로지스톤이 갇혀있던 금속 몸체가 부풀려진 것이라고도 했습니다. 물론 이는 터무니없는 주장이었습니다. 그나마 프리스틀리가 금속이 플로지스톤을 잃는 동시에 물과 결합해서 무게가 증가한다고 설명합니다.
Figure.8 라부아지에의 실험장치, 라부아지에는 부유한 귀족이었기 때문에 실험 장비도 좋았다 ⓒgallica.bnf.fr
라부아지에도 처음에는 당시 정설이었던 플로지스톤 이론으로 이 문제를 설명하고자 했습니다. 재(금속회)는 공기 물질을 포함하고 있고, 재를 태우면 그 공기 물질이 빠져나와 플로지스톤과 결합해 기체가 된다는 것이죠. 곰곰이 생각하던 라부아지에는 플로지스톤 없이도 이 과정을 설명할 수 있음을 깨닫습니다. 연소를 돕는 특정 공기가 있고, 금속을 가열하면 이 공기가 금속에 결합하고, 재(금속회)를 가열하면 이 순수한 공기가 다시 빠져나온다고 본 것이죠.
라부아지에는 이를 바탕으로 1783년 <플로지스톤에 대한 재고>를 발표하고 새로운 이론을 세웁니다. 이 새로운 이론을 알리기 위해 1789년 자신의 이론을 담은 화학 교과서 <화학원론>과 새로운 화학을 위한 학술잡지 <화학연보>를 출판합니다. 결국 플로지스톤 이론은 지지를 잃고 사라지게 되죠. 이 과정을 화학 혁명이라고 합니다.
Fig.4 원소 발견의 시대
Figure.8 (왼쪽) 라부아지에의 원소 분류표, (오른쪽) 베르셀리우스의 원자량표
과학기술이 발전하면서 새로운 원소들이 계속해서 발견됩니다. 19세기 초에는 전기분해 기술이 등장하면서 셀레늄, 토륨, 지르코늄, 타이타늄, 바륨, 칼슘, 스트론튬, 마그네슘 등이 발견되었고요. 분광법과 방사선을 통해 폴로늄, 라듐, 악티늄, 프로탁티늄, 하프늄, 레늄 등이 발견되었죠.
발견되는 원소가 많아지면서 화학자들은 분류를 시도하게 됩니다. 그 시작도 1789년 라부아지에였죠. 그는 33종의 원소들을 기체, 금속, 비금속, 토류로 분류했습니다. 1826년 베르셀리우스Jöns Jakob Berzelius 는 49종의 원소를 원자량표로 만들었죠. 그리고 이제 원소의 성질 분류와 원자량표를 합친 주기율표가 등장하게 됩니다.
Fig.5 원소도 꿰어야 주기율표
Figure.9 샹쿠르투아스의 주기율표, 표 가운데 텔루륨이 있어 텔루륨 나선이라고 불린다
성질 분류에 따른 표, 그러니까 주기율표의 첫 등장은 1862년 샹쿠르투아스Alexandre-Emile Béguyer de Chancourtois 에 의해서입니다. 그는 원소를 원자량 순서로 나열하고 이를 원통으로 만들면 되베라이너Johann Wolfgang Döbereiner 의 3원소에 속하는 원소들이 같은 위치에 놓인다는 것을 발견한 것이었죠.
되베라이너의 3원소란 물리적 특성이 유사하게 관련되어 있는 세 개의 원소 그룹이 있으며, 그 중심 원소 원자량은 나머지 두 원소 원자량의 평균값을 가진다는 것입니다. 예를 들어 리튬, 소듐, 포타슘은 알칼리 형성 원소 그룹인데 소듐의 원자량(23.0)은 리튬(7.0)과 포타슘 원자량(39.0)의 평균값이라는 것이죠.
Figure.10 뉴랜즈의 주기율표. 뉴랜즈는 멘델레예프와 아이디어를 주고 받았다고 한다
존 뉴랜즈John Newlands 는 원자량의 순서로 배열한 주기율표를 제안합니다. 그는 1865년에 당시 알려져 있던 62개의 원소를 원자량 순서로 나열하되 여덟 번째 원소마다 비슷한 성질을 가진다는 ‘옥타브 법칙’을 발표했습니다. 이는 오늘날의 주기율표와 유사한 것이죠. 그러나 당시 학계 사람들은 말도 안 된다며 조롱했고 뉴랜즈는 화학계를 떠납니다.
Figure.11 멘델레예프의 개정된 주기율표. ?표시는 당시 발견되지 않은 원소
오늘날의 주기율표는 1868년 멘델레예프Dmitry Ivanovich Mendeleyev 가 고안해 냅니다. 당시에는 모두 63종의 원소가 알려져 있었는데, 이들을 원자량의 순서로 배열할 때 주기적 성질이 있음을 발견하고 <원소 원자량과 그 성질 사이의 관계>라는 제목으로 발표했죠. 1871년에는 앞서 발표했던 주기율표를 수정하여 <원소들의 자연적 체계>라는 논문으로 발표했습니다. 여기에서 알루미늄, 실리콘, 보론 아래에 빈칸을 두어 아직 발견되지 않은 원소가 채워질 것이라고 예상하고 각각의 원자량을 예측했죠. 각각 1875년 갈륨, 1879년 스칸듐, 1886년 게르마늄이 멘델레예프가 예상한 원자량으로 발견되면서 이 주기율표의 위상이 높아졌습니다. 오늘날에도 멘델레예프의 주기율표에 따라 새로운 원소를 예측하며 발견하고 있죠.
Fig.6 중요한 건 원자량이 아니라 전하량이야
멘델레예프는 원소의 주기적 성질이 무엇때문에 나타나는 지는 알지 못했는데, 이는 1913년 모즐리Henry Gwyn Jeffreys Moseley 가 밝혀냅니다.
모즐리는 전자빔을 원소에 쏘아서 나오는 X선 스펙트럼을 연구했습니다. 연구 결과 X선 스펙트럼의 파장이 원자핵 전하와 비례한다는 것을 밝혀내죠. 이로서 주기율표의 기준은 원자량이 아닌 원자핵의 (+) 전하량으로 해야 한다는 것이죠. 원자번호로 주기율표를 재구성하자 모즐리는 원자번호 43번, 61번, 72번, 75번이 비어 있다는 것을 알게되고, 이들은 1923년 72번 하프늄, 1925년 75번 레늄, 1937년 43번 테크네튬, 1945년 61번 프로메튬으로 발견됩니다.
모즐리의 X선 실험으로 원소의 원자번호를 쉽게 결정할 수 있었는데요. 희토류의 전문가 조르주 위르뱅Georges Urbain 은 네 종류의 희토류 원소가 섞여 있는 시료를 모즐리에게 가져다주었는데, 자기가 몇 년을 고생해서 연구했던 결과를 모즐리가 불과 몇 시간 만에 분석해내서 놀라기도 했죠.
현대 주기율표를 완성시킨 모즐리는 1차 세계대전이 발발하자 자원해서 입대했고, 1915년 갈리폴리에 투입되어 전사하고 맙니다.
Fig.7 연금술(물리)
지구에 자연 상태로 존재하는 원소의 발견은 1939년 프랑슘의 발견이 마지막으로 총 92종의 자연 원소가 있습니다. 그 이후부터는 원소를 입자를 빛의 속도에 가깝게 쏘아 서로 충돌시키는 입자가속기를 통해 만들어낸 인공원소들이죠. 최초의 인공원소는 테크네튬으로 1937년 만들어졌습니다. 1944년 아메리슘과 퀴륨, 이후 멘델레븀, 뢴트게늄 등이 만들어지며 주기율표에는 총 118개의 원소가 기록되어 있습니다.
인공원소들이 자연 상태에서 관찰되지 않는 이유는 반감기가 짧기 때문입니다. 뢴트게늄은 반감기가 10여 분이고, 118번 오가네손은 단 0.00069초, 테네신은 0.00051초 마다 절반씩 사라지죠. 이렇게 순식간에 사라지는 인공원소를 만드는 이유는 우주에 존재하는 물질의 구조와 기원을 이해하는데 도움이 되기 때문입니다. 또한 인공원소인 테크네튬은 방사성 영상 진단 기술에, 아메리슘은 화재 경보기에 쓰이며 실생활에 도움이 되기도 합니다.
여기까지 내용을 요약해보자면,
0. 화학의 역사는 목적에 따라 ① 물질은 무엇으로 이루어져 있을까? ② 원소는 어떻게 결합할까? ③ 원소는 어떤 구조로 결합할까? ④ 원자는 어떻게 생겼을까? ⑤ 새로운 물질을 만들자! 로 나뉠 수 있습니다.
1. 물질은 무엇으로 이루어져 있을까?에 대한 답으로 고대 사람들은 물질은 물(1원소설) 혹은 물, 불, 흙, 공기(4원소설) 혹은 물과 공기(2원소설) 등으로 구성되어 있다고 생각했습니다.
2. 로버트 보일은 1~4개의 원소로만 물질이 이루어졌다는 고대의 원소설을 부정하고, 현대적인 원소 개념을 기반으로한 학문으로써 화학을 정립합니다.
3. 18세기에는 특히 기체 원소들의 발명이 두드러졌는데, 당시 정설로 받아들여지고 있던 플로지스톤 이론에 따라 각 원소들이 정의되고 명명되었습니다.
4. 하지만 라부아지에가 플로지스톤 이론을 무너트리면서 기체 원소들은 새롭게 정의되고 명명되었죠.
5. 새로운 원소들이 계속해서 발견되면서 원소들을 분류하는 시도가 이어지는데요. 원자량 순서로 나열하면서 되베라이너의 3원소, 옥타브 규칙 등 새로운 규칙이 발견되고, 마침내 1871년 멘델레예프에 의해 오늘날의 주기율표가 완성됩니다. 이를 통해 아직 발견되지 않은 원소들도 예측할 수 있게 되었습니다.
6. 오늘날에는 입자가속기를 이용해 원소를 인공적으로 만들어내는데요. 그렇게 해서 발견된 원소는 총 118개이죠.
Reference.
•
장홍제. (2021). 화학연대기. EBSBOOKS
572페이지의 두꺼운 분량을 가지고 있어 처음에는 선뜻 손이 안갔던 책이었는데요. 나중에는 이 책을 중심으로 뉴스레터를 작성했습니다. 그 만큼 화학사에 대해서는 정말 모든 것을 다루고 있고, 과학자에 대한 TMI들도 많이 나와서 재밌어요. 앞으로 다른 과학사 준비할 때도 많이 참고하게 될 것 같습니다.
•
윌리엄 H. 브록. (2017). 화학의 역사. 교유서가
교유서가 첫단추 시리즈의 과학철학을 좋게 읽었던 터라 기대했지만, 번역투 때문에 읽기 힘들었습니다. 참고하긴 했지만 처음 화학사를 접하는 사람에게는 추천하지는 않습니다.
•
장하석. (2017). 과학, 철학을 만나다. 지식플러스
과학철학에 이어 또 다시 참고한 책입니다. 전에도 말씀드렸다시피 쉬운 문체와 풍부한 사례를 들어 쉽게 읽힙니다. 내용도 가볍지 않고요. 화학 혁명에 대한 내용도 이곳에서 많이 참고했습니다. 제 뉴스레터에서는 다루지 않았지만 '물이 과연 100도에서 끓는가?'에 대한 내용도 추천합니다
•
장홍제. (2022). [제257호 과학학술: 8주기 원소를 찾아서] 새로운 도전, 8주기 인공원소. 경희대학교 대학원보. URL : https://khugnews.co.kr/?p=4775
•
최정모.(2022~).[화학칼럼] 화학사 돌아보기. 화학세계.
•
Nalnarioppa. 화학사. 네이버 블로그. URL : https://blog.naver.com/nalnarioppa/222013461003
* 위 버튼의 링크로 구매가 이루어지면 저에게 소정의 수수료가 지급됩니다. 항상 응원해주셔서 감사합니다.
고등학교 때 배운 화학은 틀렸다?! 화학의 역사 ② 원소는 어떻게 결합할까?
Comment.
•
제목에 어그로를 끌어봤는데요. 실제로 어느정도 맞는 말입니다(ㄴ(°0°)ㄱ) 고등학교 때 이과였다면 존 돌턴이 원자 개념을 처음 제시했다고 들었을 것이고, 화학결합을 점으로 표시하는 루이스 모델이 맞는 것으로 알고 있었을 거니까요. 무엇이 틀렸는 지는 오늘 글을 끝까지 보시면 아실 수 있습니다:)
•
우리 주변에 있는 물질은 원소가 아닌 화합물로 이루어져 있습니다. 당장 제 옆에 있는 플라스틱 물컵만 해도 탄소, 수소, 산소로 이루어진 화합물이죠. 지난주 화학의 역사에서는 물질의 근원인 원소를 찾고 분류하는 과정을 소개해 드렸는데요. 이번 시간은 원소가 어떻게 화합물이 되는지에 대한 비밀을 풀어가는 과정입니다.
•
<사소하지 않은 것들의 역사>가 너무 어렵고 늘어진다는 피드백이 있어서 기존에 계획했던 화학의 역사 분량을 조금 줄이고자 합니다. 그외에도 좀 더 쉽고 재밌게 읽으실 수 있도록 방안을 모색하고 있는데요. 혹시 좋은 아이디어가 있으시다면 여기로 남겨주세요
Fig.1 괴테에게 영감을 준 친화력
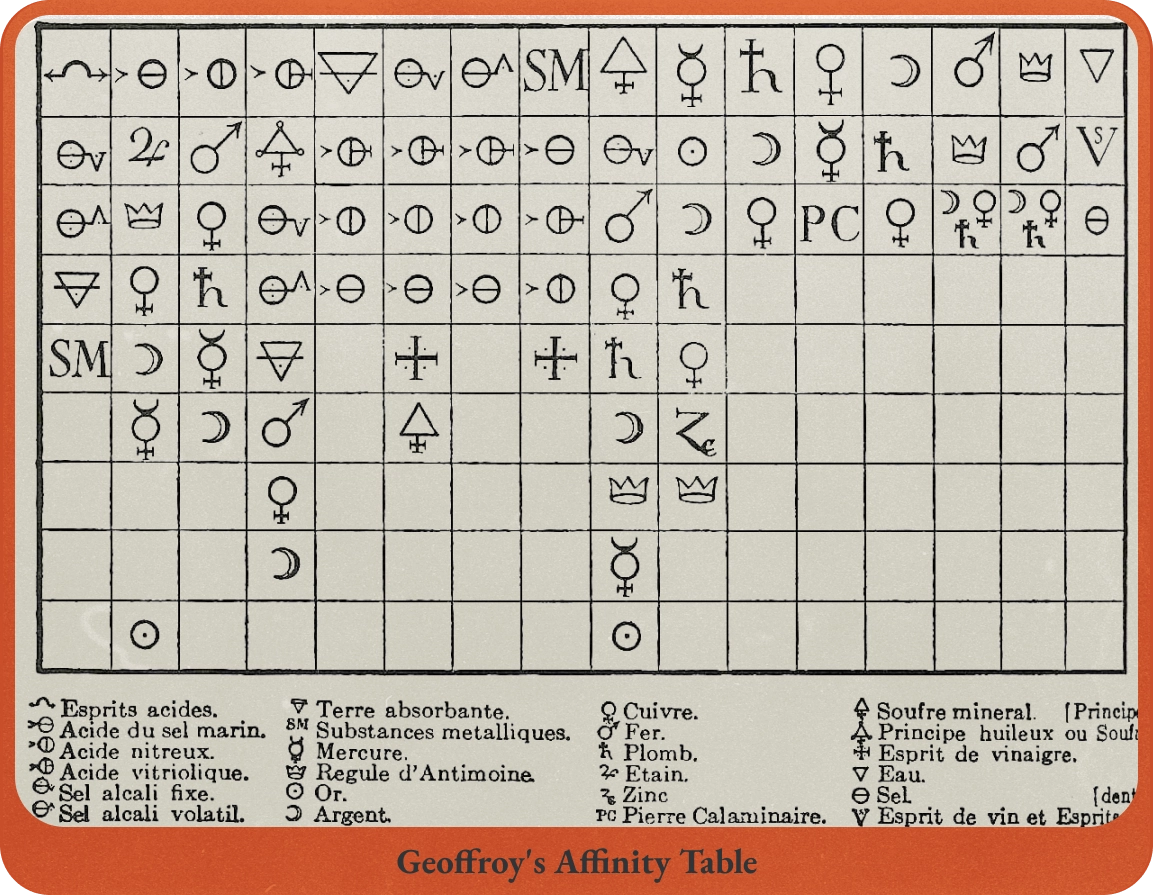
Figure.1 조프루아의 친화력표 - 각 열에 있는 원소끼리 결합가능하다
연금술사와 초기 화학자들은 두 종류의 화합물이 반응하여 원래의 화합물이 분해되고 새로운 화합물이 생기는 현상을 보고 원소 간의 결합에 우선순위가 있다는 생각을 하게 됩니다. 이를 친화력이라고 불렸죠. 1718년에는 에티엔 프랑수아 조프루아 Étienne François Geoffroy 가 원소들의 친화력을 정리하여 <친화력표>를 발표합니다. 이 표는 약산에 다른 산을 넣어 화학반응을 일으키는 양을 측정하여 작성한 것이었죠. 이 과정에서 조프루아는 황 성분을 찾아내 친화력표에 포함했는데요. 그는 이 황을 플로지스톤이라고 생각했습니다.
Figure.2 토르베른 올로프 베리만
조프루아의 친화력표는 16열로 구성되어 있었는데요. 친화력표는 점차 발전하여 1781년 토르베른 올로프 베리만Torbern Olof Bergman 이 발표한 친화력 표에서는 50열이 넘어가게 됩니다. 이 베리만의 연구를 보고 영감을 얻은 괴테는 1809년 <친화력>이라는 소설을 발표하기도 했죠.
Fig.2 화합물은 일정 성분비로 결합한다?! - 프루스트 vs 베르톨레
Figure.3 프루스트와 베르톨레
1799년 프랑스의 화학자 프루스트Joseph-Louis Proust 는 구리가 산소와 단일한 비율로 결합해 산화구리를 형성한다는 실험 결과를 얻어냅니다. 이 결과를 기반으로 화합물은 원소의 일정한 성분비로 이루어져 있다는 사실을 처음 발표합니다.
반면 1803년 <화학 정역학론>을 출판한 베르톨레Claude Luis Berthollet 는 화합물의 반응비는 최솟값과 최댓값 사이의 임의의 값을 가질 수 있으며, 이 값은 온도, 압력, 반응물의 양 등에 의해 변화된다고 주장했습니다. 그러면서 베르톨레는 프루스트의 주장을 반박하는데요. 황화구리는 일정한 비율의 구리를 포함한 것처럼 보이지만 황철석에 포함된 구리의 비율은 제멋대로라는 것이었죠.
이는 실제 많은 화합물이 단일한 성분비로 반응하지 않기 때문이었는데요. 예를 들어 베르톨레가 말한 황화구리는 황화 구리(I)(Cu2S)과 일황화 구리(CuS) 등이 존재하죠. 프루스트도 이를 깨닫고 화학 반응에서 반응물들은 고정된 비율로 반응하지만, 그 비율이 여러 가지일 수 있다는 결론을 내립니다.
Fig.3 가장 단순한 비율로 결합한다 - 돌턴
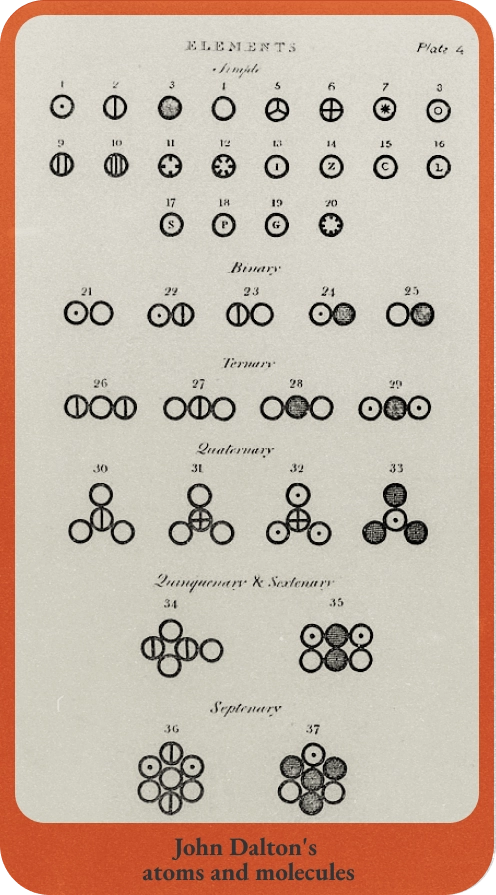
Figure.4 돌턴의 원자 모형
많은 사람이 존 돌턴John Dalton이 원자설을 처음 제시했다고 알고 있습니다. 하지만 돌턴 원자설의 입자 개념은 보일, 라부아지에도 이야기했고 심지어는 뉴턴도 1704년 발표한 <광학>에서 입자 개념을 이야기했습니다. 그럼에도 돌턴의 원자설이 이토록 유명한 이유는 무엇일까요? 그것은 바로 원자의 질량을 결정할 수 있다는 점 때문이었습니다. 이를 통해 원소주기율표도 작성할 수 있게 되었고, 그 과정에서 원소의 특성들도 알 수 있게 된 것이죠.
돌턴이 원자량을 구한 방법은 다음과 같습니다. 우선 돌턴은 화합물을 원소들이 가장 단순한 비율로 결합한다고 가정합니다. 당시 알려져 있던 화합물을 전부 조사하여 그 중 ‘비율이 가장 작은 화합물은 1:1’로 결합한다고 가정한 것이죠. 가령 돌턴에 의하면 물은 수소와 산소가 1:1 비율로 결합합니다. 그리고 당시 과학자들은 실험을 통해 물에서 산소와 수소의 비율이 약 7:1이라는 사실을 알고 있었죠. 따라서 산소와 수소가 1:1로 결합한다고 했으니 무게비도 7:1이 되죠. 이런 식으로 돌턴은 수소의 무게를 1단위로 잡은 뒤 다른 원자와 분자의 무게를 유추해 냅니다.
물론 돌턴이 무턱대고 화합물이 단순한 비율로 구성되어 있다고 가정한 것은 아닙니다. 서로 다른 원자들끼리는 최대 12개까지 결합할 수 있지만, 같은 종류의 원자들끼리는 서로 밀어내는 성질을 가지고 있기 때문에 가장 안정적인 구조는 가장 단순한 비율로 결합하는 구조라고 한 것이죠.
Fig.4 부피비로 결합한다 - 아보가드로
Figure.5 게이-뤼삭
하지만 돌턴의 원자설이 화학자들에게 바로 수용된 것은 아니었습니다. 일부 화학자들은 질량이 측정량의 대표로 사용되어야 하는지에 대한 의문이 있었죠. 그래서 질량 대신 널리 사용된 측정량은 부피였습니다. 대표적인 예로 1808년 조제프 게이-뤼삭Joseph Louis Gay-Lussac 이 발표한 기체 반응의 법칙이 있죠. 이는 기체들 간에 화학반응이 일어나면 그 기체의 부피는 간단한 정수비를 이룬다는 것입니다. 예를 들어 수소와 산소를 반응시켜 수증기가 될 때 수소와 산소의 부피비는 2:1입니다.
Figure.6 아보가드로
게이-뤼삭의 기체 반응의 법칙을 본 아보가드로Amedeo Avogadro 는 입자수도 부피비가 그대로 성립할 것이라는 생각을 합니다. 즉 부피비 그대로 입자수 비가 되는 것이죠. 이를 토대로 1811년 같은 온도와 같은 압력에서 일정 부피 안에 들어 있는 입자 수는 기체의 종류와 무관하게 동일하다는 아보가드로 법칙을 제시합니다.
이를 물의 반응에 대입해보면, 당시 실험을 통해 수소와 산소를 반응시켜 물을 만들 때 수소(H), 산소(O), 물의 부피비는 2:1:2임을 알았습니다. 돌턴에 의하면 수소는 H, 산소는 O, 물은 HO니까 2H + O →2(HO)이 됩니다. 그런데 수식이 맞지 않습니다. 없던 산소가 생겨야 할판이죠. 이를 해결하기 위해서 아보가드로는 하나의 원소로 이루어진 물질은 단일 입자로 되어있지 않다고 주장합니다. 예를 들어 산소는 O가 아닌 O₂, 수소는 H가 아닌 H₂로 말이죠. 즉 물의 반응은 2H₂ + O₂ → 2H₂O가 됩니다.
하지만 아보가드로의 이론은 별다른 주목을 받지 못하고 50년간 묻혀있게 되는데요. 이후 1860년 국제 화학 회의에서 원소량을 아보가드로 법칙으로 바탕으로 결정하게 되면서 재주목됩니다.
Fig.5 화학 결합은 전기로 이루어져 있다
Figure.7 전기를 가지고 실험하는 데이비 험프리
19세기 초 화학계에서는 돌턴의 원자설과 볼타 전지가 가장 핫한 주제였습니다. 전기분해를 통해 알칼리 금속을 발견한 험프리 데이비Sir Humphry Davy 는 전기를 통해 화합물에서 원소를 분리해 낼 수 있다는 것은 반대로 화합물이 전기적인 힘으로 결합하여 있다는 것이라는 생각에 이르게 됩니다.
Figure.8 전기화학적 이원론을 체계화 시킨 베르셀리우스
1811년 베르셀리우스 Jöns Jakob Berzelius도 마찬가지로 화학 친화력이 전기적 현상이라는 가설을 제시합니다. (+)인 원자와 (-)인 원자가 결합해 화합물을 형성하고, 이 때 두 원자의 비율은 중성을 만들 수 있는 최소한의 비율이라는 거죠. 이를 전기화학적 이원론Dualism 이라 부릅니다.
다만 전기적 이원론은 유기화학에서 설명이 어려웠고, 또한 O₂와 같이 단일 원소로 이루어진 물질에 대해서는 어떻게 전기적 성질이 같은 물질이 결합을 이룰 수 있는지 설명하지 못했죠.
Fig.6 전자가 공유된다
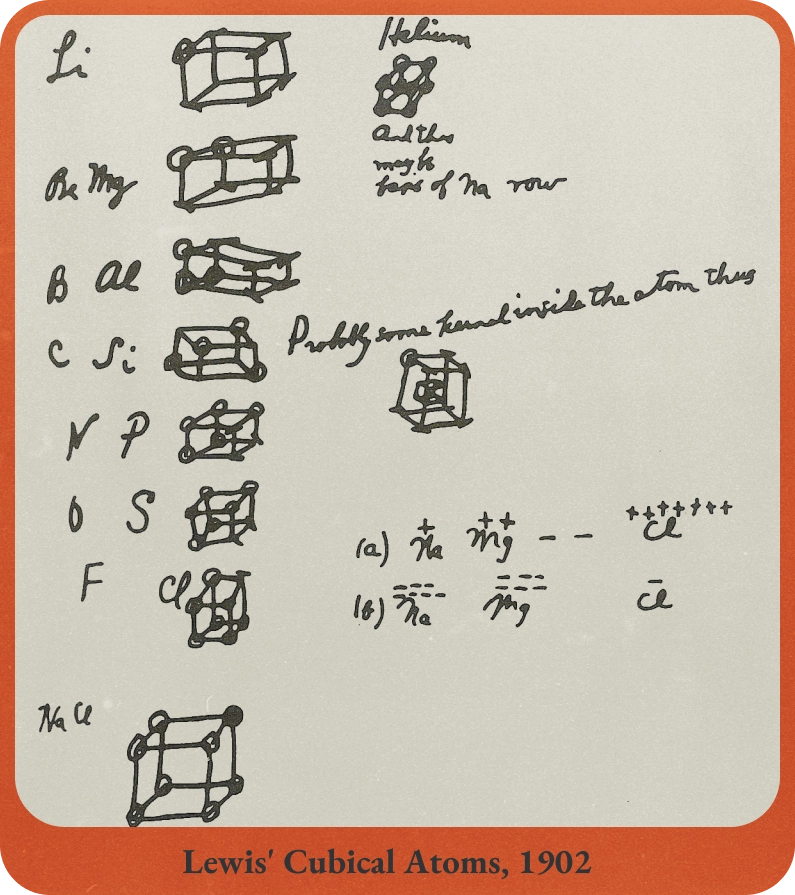
Figure.9 루이스의 입방체 원자 모델의 아이디어 노트
1897년 톰슨이 전자를 발견하고, 러더퍼드가 1911년 원자핵을 발견하면서 점차 원자 결합 모델에 대한 실마리가 잡힙니다. 이를 바탕으로 1916년 길버트 루이스Gilbert Newton Lewis 는 <원자와 분자의 화학결합> 논문에서 원자의 바깥 전자를 입방체 꼭짓점에 배치하는 입방체 원자 모델을 선보입니다.
그리고 안정한 분자들이 대부분 짝수 개의 전자를 갖는다는 것을 보고 전자쌍 결합 아이디어를 제시하죠. 전자쌍 결합이란 화합결합은 각 원자의 전자가 쌍으로(2개씩) 공유되어 이루어진다는 것입니다. 이렇게 전자 2개를 공유하면서 만들어진 화학결합을 '공유결합'이라고 했죠.
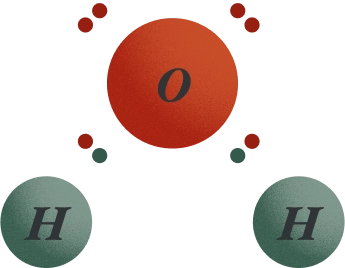
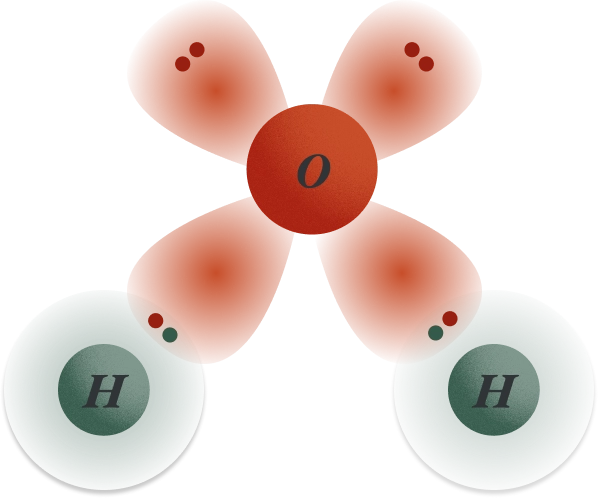
Figure.10 루이스의 전자쌍 결합으로 표현한 H₂O,
6개의 전자를 가진 산소와 1개의 전자를 가진 수소
사실, 화학 결합이 원자들 사이의 전자 공유로 이루어진다는 주장은 수많은 과학자가 제시했습니다. 하지만 이들은 결합에 관여하는 전자 개수와 전자 공유에 동시에 참여하는 원자 수를 제시해 주지 못했죠. 반면, 루이스는 하나의 결합을 형성하기 위해 필요한 전자 개수는 2개, 하나의 결합에 관여하는 원자 수는 2개로 명확하게 제시함으로써 유용하게 활용할 수 있는 모델이 될 수 있었죠.
루이스 모델은 오늘날에도 화학결합을 이해하기 위해 배우는 유용한 모델이지만, 양자역학이 발전하면서 실제와는 다르다는 것이 밝혀집니다. 루이스 모델에서는 전자를 점으로 표현했지만, 양자역학(불확정성 원리, 파동함수 이론)에 의하면 전자는 점으로 찍을 수 없고 공간상에 퍼져 있습니다. 또한 전자 2개가 공유되면 화학결합이 안정화된다는 것은 양자역학(슈뢰딩거 방정식)으로 설명되지 않죠.
Fig.7 양자역학이 왜 여기서 나와요
Figure.11 원자가결합이론으로 표시한 H₂O, 위치함수가 겹치는 곳이 공유결합이 이루어진 곳이다.
화학결합을 최초로 양자역학적으로 설명한 것은 1927년 하이틀러Walter Heinrich Heitler와 런던Fritz Wolfgang London 입니다. 이들은 수소분자의 화학결합을 양자역학적으로 설명해내죠. 곧이어 슬레이터John Clarke Slater 와 폴링Linus Pauling이 하이틀러-런던 법을 일반화합니다. 이렇게 해서 등장한 것이 루이스 모델을 양자역학적으로 보완한 원자가결합이론(Valence-Bond Theory, VBT)입니다.
원자가 결합 이론을 간단히 설명하면 전자를 특정 시간, 특정 위치에 있을 확률을 나타내는 함수(오비탈)로 표현해, 각 전자의 함수가 겹치면 공유결합이 이루어진다는 것입니다.
다만 루이스 모델에서 발전된 만큼 결합에 직접 참여하는 전자만을 대상으로 하고, 전자가 특정 위치에 치우쳐있다고 가정하는데요.(결합에 참여하는 전자는 두 핵 사이에 놓이지만, 하나의 핵에 속한 상태를 가정) 이 때문에 실제 분자 구조를 설명하기 위해서 공명 등의 추가적인 개념이 필요하죠.
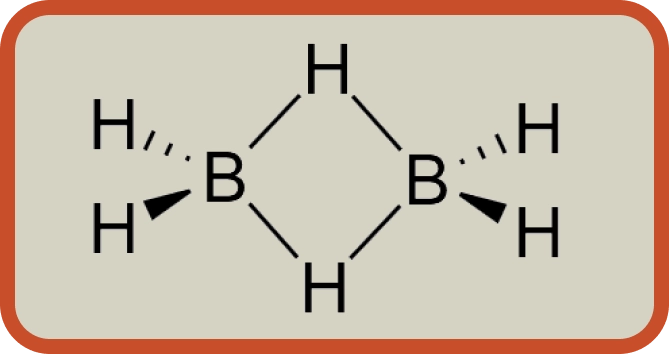
Figure.12 다이보레인, 두 개의 팔을 가지고 있는 가운데 수소(H)들
또한 원자가 결합 이론으로 설명하지 못하는 것들이 있었는데요. 대표적인 예로 붕소 원자 2개와 수소 원자 6개가 결합한 다이보레인(B₂H₆)이 있습니다. 수소 원자는 전자를 한 개 가지고 있어 루이스 모델에 의하면 팔이 하나여야 하는데요, 다이보레인은 가운데를 보면 수소가 2개의 팔을 가지고 있죠.
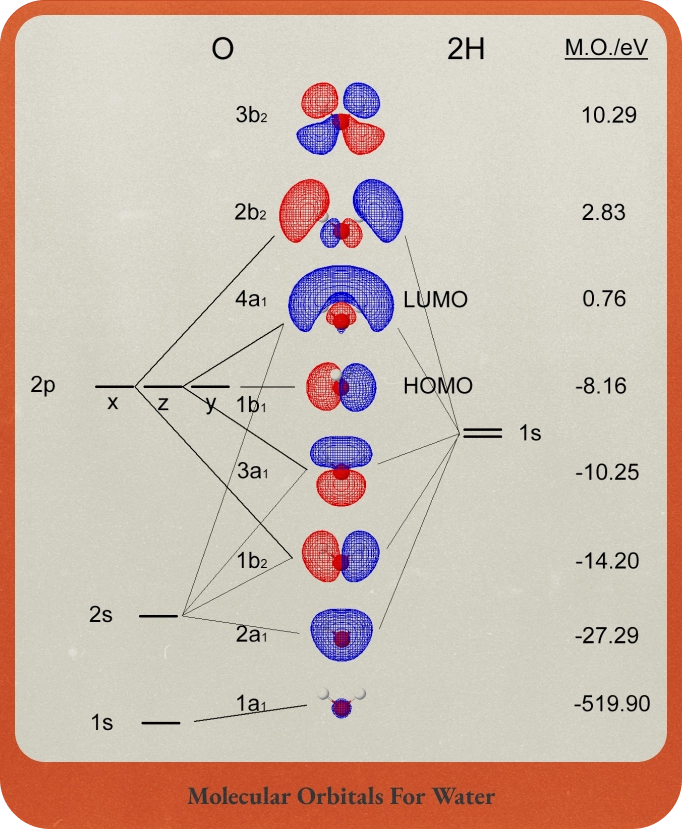
Figure.13 분자 오비탈 이론으로 표현한 물의 결합
이러한 원자가 결합 이론의 한계를 보완하기 위해 1929년 프리드리히 훈트Friedrich Hund 와 로버트 멀리컨Robert S. Mulliken 가 분자 오비탈 이론(MOT, Molecular Orbital Theory)을 제시합니다. 분자 오비탈 이론(MOT)은 원자가 결합 이론(VBT)과 달리 모든 전자가 분자 전체에 걸쳐 고르게 퍼져있다고 가정합니다. 따라서 모든 전자가 동등하게 상호작용하죠.
여기까지 내용을 요약해보자면,
1. 초기 화학에서는 원소 간의 결합에 우선순위가 있다는 친화력을 주장했습니다. 이에 조르푸아, 베리만 등이 친화력표를 작성하죠.
2. 프루스트와 베르톨레는 화합물이 원소의 일정비율로 결합되는지에 대해 논박을 벌이는데요. 결국 일정성분비로 이루어져있다는 주장을 한 프루스트의 주장이 옳았음이 밝혀지죠.
3. 돌턴은 원자설을 통해 원소는 가장 단순한 비율로 결합해 화합물을 이룬다고 주장합니다.
4. 반면, 아보가드로는 부피비로 결합한다고 주장하죠. 이 과정에서 이원자분자(ex. O₂, H₂)도 예측합니다.
5. 19세기 초 등장한 전자기학을 통해 데이비와 베리셀리우스가 화학 결합은 전기적 현상이라는 이원론을 주장합니다. 하지만 이원론은 유기화학과 이원자분자에서 설명이 어려웠죠.
6. 20세기 초 원자 구조가 점차 밝혀지면서 루이스가 화합결합은 원자들 사이에 전자를 공유하면서 이루어진다는 루이스 모델을 제시합니다. 하지만 루이스 모델은 양자역학을 등장하면서 틀린 부분이 있음이 밝혀집니다.
7. 하이틀러, 런던, 슬레이터, 폴링은 루이스 모델을 양자역학적으로 발전시켜 원자가결합이론을 제시합니다. 하지만 원자가 결합이론은 루이스 모델의 가정을 따르기 때문에 여러 문제가 있었고 이를 보완하기 위해 훈트와 멀리컨이 분자 오비탈 이론을 제시합니다.
Reference.
•
김지환. (2018). 분자사용설명서. 반니
•
원서읽기연구소. (2013). 원서보다 먼저 읽는 영어로 화학. 이다새(부키)
•
윌리엄 H. 브록. (2017). 화학의 역사. 교유서가
•
장하석. (2017). 과학, 철학을 만나다. 지식플러스
•
장홍제. (2021). 화학연대기. EBSBOOKS
•
짐 배것. (2014). 퀀텀스토리. 반니
•
최정모.(2022~).[화학칼럼] 화학사 돌아보기. 화학세계.
•
Nalnarioppa. 화학사. 네이버 블로그. URL : https://blog.naver.com/nalnarioppa/222013461003
이걸 알아야 양자역학 이해됨 화학의 역사 ③ 원자는 어떻게 생겼을까?
Comment.
•
원자의 구조는 아주 미시 세계의 이야기이기 때문에 양자역학으로 이어집니다. 그래서 원자의 구조를 화학의 역사가 아닌 물리학의 역사를 조사할 때 다룰까 고민했었는데요. 원자의 구조를 밝히는 데 크게 기여한 러더퍼드 선생님께서 본인은 “자연과학은 물리학과 우표수집 둘로 나누어진다”라고 말하시고는 노벨 우편수집(화학)상을 받으시는 것을 보고 화학의 역사에서 다루기로 결심하게 되었죠.
•
원자 구조 이론과 양자역학은 1910~20년대에 급격하게 발전합니다. 같은 시기에 무슨 일이 있었나 살펴보았는데 1차 세계대전과 러시아 혁명이 있었고, 정신분석학이 유행했으며, <벤자민 버튼의 기이한 사건>, <위대한 개츠비>, <데미안>이 출간된 시기이기도 하더라고요. 미국은 대공항 직전의 호황기로 재즈와 스포츠 등의 대중문화가 발전했었죠. 여러모로 대격변의 시대였던 것 같네요.
Fig.1 전자의 발견
Figure.1 가운데 전극을 걸어주자 휘는 음극선
19세기 초 과학계의 핫이슈는 단연 전기였습니다. 1869년 율리우스 플뤼커Julius Plücker 는 진공상태의 유리관에서 (-)극에서 (+)극으로 어떤 광선 같은 것이 흐른다는 것을 발견합니다. 이 흐름이 음극에서 시작되기 때문에 ‘음극선’이라 불렀죠. 이 음극선이 무엇인지 추측이 난무하는 가운데 조지프 존 톰슨Sir Joseph John Thomson 은 이 음극선 가운데 전극을 걸어주는 실험을 합니다. 실험 결과 음극선이 (+)극 쪽으로 휜다는 사실을 발견하죠. 즉 음극선은 (-)를 띤다는 겁니다.
톰슨은 실험을 이어나가는데, 또 다른 실험에서는 유리관 속에 얇은 금속으로 만든 물레방아 같은 장치를 설치합니다. 이 물레방아에 음극선을 쏘았더니 물레방아가 돌아가는 것이 관찰되었죠. 즉 음극선은 단순한 빛이 아니라 물리적인 실체가 있다는 것이죠.
톰슨은 음극선의 전하량을 측정하여 음극선에서 나오는 물질의 질량이 가장 가벼운 원소인 수소보다 약 1,800배 가볍다는 것을 보임으로서 이것이 원자가 아니라 새로운 입자임을 증명합니다. 그리고 이 입자에 전자라는 이름이 붙여졌습니다.
Figure.2 전자가 건포도처럼 박혀있는 톰슨의 원자 모형
전자를 발견한 톰슨은 원자는 (+)전하가 고르게 분포된 원 안에 전자가 건포도처럼 박혀있는 것이라고 주장합니다. 이를 푸딩 모델이라고 하죠. 하지만 푸딩 모델로는 물체가 자기적 성질이 나타내는 것을 설명할 수 없었습니다. 푸딩 모델에서 전자가 움직이면 원자는 불안해져 원래의 형태를 유지를 유지할 수 없거든요.
Fig.2 원자 핵의 발견
이 문제를 해결한 것이 톰슨의 제자였던 어니스트 러더퍼드Ernest Rutherford 입니다. 참고로 러더퍼드는 “자연과학은 물리학과 우표수집 둘로 나누어진다”라고 말하고 노벨 우편수집(화학)상을 수상한 것으로 유명하죠.
러더퍼드는 주요 연구주제는 방사선이었습니다. 러더퍼드는 방사선이 원자 내부의 붕괴에 의해 방출된다는 사실을 알아내고, 우라늄과 토륨에서 투과력이 약한 알파선과 투과력이 강한 베타선을 발견합니다.
Figure.2 알파선 실험. 원자핵에 부딪힌 알파입자는 튕겨져 나온다
1908년 러더퍼드는 본인이 발견한 알파선을 얇은 금박에 발사하여 알파 입자의 궤적이 어떻게 되는지 측정하는 실험을 설계합니다. 러더퍼드는 알파선이 투과력을 가지고 있기 때문에 얇은 금박을 투과하고 전자에 의해서 살짝 휘는 것을 예상했는데요. 그런데 예상치 못하게 튕겨져 나온 알파 입자가 관측되었습니다. 이 말인즉슨 얇은 금박에 알파 입자가 부딪혀 튕겨져 나올만큼 무거운 무엇인가가 있다는 뜻이었죠. 이렇게 원자 핵의 존재를 밝혀냅니다.
Figure.3 전자가 원자핵 주변을 공전하는 러더퍼드의 원자 모형
그렇다면 강한 전하량을 가지고 있는 원자 핵에 작은 전자가 들러 붙지 않는 이유를 찾아야 했는데요. 러더퍼드는 전자가 계속해서 공전해 중심으로 빨려들어가지 않는다고 주장합니다. 하지만 전하를 띤 입자가 전자기장 속에서 움직이면 에너지가 방출됩니다. 즉 전자가 원자핵 주변을 공전하고 있다면 전자는 에너지를 잃으면서 궤도 반경이 작아지고 결국 원자핵으로 빨려들어가 붕괴되어야 합니다.
Fig.3 전자 궤도는 정해져 있다
러더퍼드 원자모델의 문제를 해결하는 것은 닐스 보어Niels Henrik David Bohr 입니다. 1911년 20살이었던 보어는 장학금을 받고 톰슨의 연구실에 들어가는데, 지도교수였던 톰슨과 처음 만나는 날 톰슨 원자 모형의 틀린 부분을 지적합니다. 시작부터 지도교수에게 찍힌 보어는 러더퍼드 연구실로 도망(?)치게 됩니다. 어쩌면 그때부터 새로운 원자 모형을 제시할 운명이었던 것이 아니였나 싶습니다.
보어는 러더퍼드 원자 모형의 문제점인 원자의 붕괴 역설을 해결하기 위해 전자가 원자핵 주변을 공전할 수 있는 안정된 배치가 존재한다는 가설을 세웁니다. 하지만 이를 입증할 현상이 없었는데요. 이 문제로 고민하던 중 보어는 동료로부터 우연히 발머Johann Jakob Balmer 의 연구에 대해 듣게 됩니다.
Figure.4 수소의 선 스펙트럼에 나타나는 에너지와 보어 원자 모형의 궤도
발머의 연구는 다음과 같습니다. 당시 원자가 방출하거나 흡수하는 에너지(전자기파)를 분석하는 스펙트럼 선 연구가 꾸준히 진행 중이었는데요. 수소의 스펙트럼을 분석한 결과, 스펙트럼의 특정 부분만 표시된다는 것을 알게 됩니다. 그리고 1884년에 발머가 수소 스펙트럼 선에서 규칙을 발견하죠.
보어는 이 발머의 연구를 보고 수소 스펙트럼 선에 나타난 선이 전자가 궤도를 돌다가 작은 궤도로 떨어질 때 방출되는 에너지라고 생각합니다. 즉 궤도 사이의 에너지 차이가 고정되어 있으니 궤도가 고정되어 있다는 것이죠. 이와 같은 내용은 1913년 <원자와 분자의 구조에 관하여>라는 논문으로 출판합니다.
Fig.4 전자는 입자이자 파동이다
보어는 양자역학을 원자 구조 설명에 도입함으로서 혁신을 이루긴 했지만, 러더퍼드의 원자 붕괴 역설을 완전히 해결한 것은 아니였습니다. 특히 특정 궤도에만 전자가 존재한다는 가설에 대한 근거를 대지 못했죠. 이를 루이 드 브로이Louis de Broglie 가 창의적인 발상으로 간단하게 해결합니다.
드 브로이는 1924년 빛이 입자성과 파동성을 모두 가지고 있다는 데에 착안해, 물질도 이중성을 갖고 있다는 가설을 수학적으로 유도해내 노벨 물리학상을 받았죠. 드 브로이는 원자 모형 속의 전자의 움직임을 파동으로 설명합니다.
Figure.5 기타줄에서 파동의 예시
우선 이해를 돕기 위해 기타줄을 튕기는 것을 상상해봅시다. 기타줄은 양끝이 고정되어 길이가 정해져있죠. 이처럼 파동 전체의 길이가 고정되어 있는 경우, 파동은 줄 길이의 정수배로 나눠지는 길이의 파동만 가능합니다. 이런 파동을 정상파라고 하죠.
Figure.6 파동으로 설명하는 보어의 원자 궤도
그럼 다시 보어의 원자 모형으로 돌아가 보겠습니다. 전자를 입자가 아닌 파동 그러니까 궤도 전체로 보면 길이가 정해져 있는게 되고 전자의 파장의 정수배가 되는 정상파 궤도만이 가능하게 되죠.
Fig.5 자세히 보니 선이 여러개네?
Figure.7 네온의 선 스펙트럼, 넷플릭스 인트로 아님. 여러 선으로 보이는 제이만 효과를 볼 수 있다
그런데 수소 스펙트럼 선은 자기장을 걸어주면 여러 개의 선으로 갈라집니다. 이는 전자가 발견되기도 전인 1897년 피터르 제이만Pieter Zeeman 이 발견해 제이만 효과라고 하죠. 연구가 계속 되면서 원자의 스펙트럼이 갈라지는 양상이 더 복잡하다는 사실을 알게 되었습니다. 그 중 스펙트럼선이 셋으로 갈라지는 경우를 정상 제이만 효과, 그 이상으로 갈라지는 현상을 이상 제이만 효과라고 부르죠. 보어의 원자 모델로는 제이만 효과를 설명할 수 없었습니다.
Figure.8 조머펠트 이론의 시각적 설명 ⓒ 석군의 비밀수납장 유튜브
아르놀트 조머펠트Arnold Sommerfeld 는 제이만 효과를 해결하기 위해 보어의 원자 모형을 분석합니다. 보어의 원자모델은 전자의 운동을 원으로 그리고 있는데요. 궤도의 에너지 총합만 같다면 전자는 여러 궤도를 가질 수 있다는 생각에 이르러 타원 궤도를 도입합니다.
기존 보어의 원자모형에서 에너지 크기에 따라 전자가 위치할 수 있는 궤도를 주양자수라고 부르는데요. 여기에 조머펠트는 하나의 주양자수가 가질 수 있는 여러 모양의 궤도를 부양자수라고 합니다. 그리고 각 궤도는 3차원 공간에서 여러 방향을 가질 수 있는데요. 이를 표현한 값이 자기양자수라고 합니다. 조머펠트는 이 자기양자수로 제이만 효과를 설명하죠. 이것을 보어-조머펠트 이론이라 부릅니다.
하지만 보어-조머펠트 이론으로는 홀수 개의 제이만 효과만 설명 가능하고 짝수 개가 나타나는 경우는 설명할 수 없었죠.
Fig.6 ??? : 그래도 전자는 돈다
Figure.9 보어의 원자모형으로 만들어진 현대식 주기율표
보어는 자신의 원자 모형을 통해 주기율표를 설명하고자 했습니다. 만약 보어-조머펠트의 이론이 옳다면 주기율표에 있는 모든 원자들을 설명할 수 있어야 했죠. 보어의 이론을 토대로 주기율표는 현재의 모습을 갖게 되는데요. 주기율표에서 세로축은 궤도 수에 해당하고, 가로축은 각 궤도에서 전자가 위치할 수 있는 개수를 의미하죠. 그런데 보어는 주기율표 줄 별로 위치한 원자의 갯수, 그러니까 첫째 줄에 2개, 두세번째 줄은 8개, 네다섯번째 줄엔 18개, 여섯•일곱번째 줄엔 32개의 의미가 무엇인지 밝혀낼 수 없었습니다.
1924년 에드먼드 스토너Edmund Clifton Stoner 는 이 숫자가 자기양자수의 2배를 하면 나온다는 것을 깨닫고 <원자 에너지 준위 사이의 전자 분포>라는 논문으로 발표하죠. 이 논문을 본 볼프강 파울리Wolfgang Ernst Pauli 는 자기양자수에 대응하여 쌍으로 존재하는 새로운 양자수가 있어야 한다고 생각합니다. 이를 "고전적으로는 표현할 수 없는 2가”라고 불렀고 1925년 논문으로 발표합니다.
그렇다면 파울리가 말한 쌍으로 존재하는 마지막 양자수란 무엇일까요? 이에 대한 비밀은 대학원생이었던 호우트스미트Samuel Goudsmit 와 울렌백George Uhlenbeck 이 풀게 됩니다.
Figure.9 전자의 자전
우선 원자핵을 돌고 있는 전자를 생각해봅시다. 원자핵은 전자를 끌어당기는 힘이 있고, 전자는 이를 상쇄하기 위해 원자핵 주변을 공전하면서 원자핵이 끌어당기는 만큼의 각운동량을 만들어 가집니다. 그런데 전자가 쌍으로 존재한다고 했으므로 각각의 전자는 원자핵이 끌어당기는 힘의 1/2 만큼의 각운동량을 가지게 되죠.
그런데 전자가 하나만 존재하는 경우도 많습니다. 각운동량이 1/2밖에 없다면 전자는 원자핵으로 빨려 들어가야합니다. 이를 해결한 것이 바로 전자가 자전한다는 아이디어입니다. 즉 공전을 통해 1/2만큼의 각운동량을 가지고 자전을 통해 1/2만큼의 각운동량을 가져서 원자핵이 끌어당기는 만큼의 힘을 만들어내는 것이죠. 그러면 전자가 두 개인 경우는 원자가 당기는 힘보다 전자의 각운동량이 더 커져 떨어져 나가는 것 아니냐는 물음이 있을 수 있는데요. 이는 각 전자의 자전 방향이 반대라서 자전에 의한 각운동량이 상쇄된다는 것으로 설명합니다.
이런 아이디어를 제시한 호우트스미트와 울렌백은 자신들의 아이디어에 자신이 없었습니다. 논문을 쓸 생각도 없었죠. 지도교수인 파울 에렌페스트Paul Ehrenfest 가 이들을 격려하여 논문을 쓰도록 했죠. 겨우 논문을 쓴 울렌백은 헨드릭 로런츠Hendrik Antoon Lorentz 의 수업을 듣고 있었는데, 로렌츠에게 논문을 보여주고 조언을 구합니다. 로렌츠는 일주일 뒤에 전자가 실제로 회전을 한다면 전자 표면의 속도는 빛의 속도의 10배에 이르러야 한다는 것을 계산해오죠. 이를 듣고 호우트스미트와 울렌백은 논문을 내지 않으려고 했는데, 에른페스트는 “자네들은 젊으니까 그렇게 바보같은 짓을 좀 해도 괜찮아”라고 말하며 이미 논문을 제출했다고 말합니다. 그렇게 울렌벡과 호우트스미트의 논문은 1925년 출판되었고 폭발적인 반응을 얻죠.
Fig.7 양자역학적으로 보는 원자 구조
Figure.10 양자수에 따른 오비탈의 모양 : 주양자수 n (크기), 방위양자수 l (모양), 자기양자수 m (방향)
이로써 보어의 원자 모형은 완성됩니다. 하지만 앞서 로렌츠가 계산한 것처럼 전자가 스핀을 하면 전자 표면의 속도는 빛의 10배 속도에 이르러야 하는 등 해결하지 못하는 모순이 많았습니다. 즉 실제로 전자는 자전하지 않는다는 거죠. 이러한 문제는 양자의 세계를 고전역학으로 설명했기 때문이었습니다.
이후 하이젠베르크의 불확정성 원리, 슈뢰딩거의 파동 방정식, 막스 보른의 확률 밀도 함수으로 이어지는 양자역학의 발전으로 원자 모형도 확률적으로 표현하게 됩니다. 그것이 바로 오늘날의 오비탈 모형이죠. 오비탈이란 특정 위치에서 전자가 발견될 확률을 시각화 시킨 함수를 말합니다. 전자의 확률 분포는 주양자수, 방위양자수, 자기양자수의 영향을 받습니다. 주양자수는 오비탈의 크기, 방위양자수는 오비탈의 모양, 자기양자수는 오비탈의 방향을 결정하죠.
Reference.
•
짐 배것. (2014). 퀀텀스토리. 반니
•
이강영. (2018). 스핀. 계단.
•
김영훈. (2019). 알아두면 쓸모있는 양자역학 이야기 - 드브로이 물질파. 삼성 디스플레이 뉴스룸. URL : https://news.samsungdisplay.com/19379
•
DMT PARK. (2023, Mar 31). 원자를 이해하는 가장 우아한 방법 [Video]. YouTube. https://youtu.be/6Csu_VZ4xR0?si=lBDYK5nMIf7gZREd
•
석군 seokkun. (2019, Dec 9). 원자모형의 변천과정과 스핀 1/2편_과학_15_석군 [Video]. YouTube. https://youtu.be/afSIlrWUL7k?si=ZvX8O6xNwwYERXx1
총, 약, 플라스틱 화학의 역사 ④ 현대의 연금술, 고분자 화학
Comment.
•
화학적으로 새로운 물질을 만들어낸다는 것은 원소를 말하는 것이 아니라 고분자물질을 이야기합니다. 그리고 이러한 고분자 물질들은 필요에 의해서 그러니까 상용화하는 과정에서 만들어지죠.
•
화학을 상용화하는 모습은 화학 기업들의 역사를 보면 쉽게 파악할 수 있습니다. 가장 큰 화학 회사인 듀폰과 BASF의 역사를 간략하게 알아보자면, 듀폰의 설립자인 듀폰Éleuthère Irénée du Pont de Nemours 은 어린시절 라부아지에 밑에서 폭발물 생산 기술을 배웠는데요. 프랑스 혁명에 집안이 휘말리자 1800년 미국으로 이민을 갑니다. 그곳에서 미국산 화약의 품질이 열악한 것을 보고 화약 생산에 뛰어들죠. 이후 미국 남북전쟁 당시 북부군이 사용한 화약의 절반가량을 공급하며 대기업으로 성장합니다. 1920년대부터는 재료 과학에 투자하며 이후 네오프렌, 나일론, 테프론 등을 발명하며 사업을 이어가죠.
•
BASF를 설립한 프리드리히 엥겔호른Friedrich Engelhorn 은 원래 가스등에 사용되는 가스를 공급하는 회사를 운영했습니다. 가스 생산 과정에서 부산물로 콜타르가 나오는데, 콜타르에서 염료를 만들어낼 수 있다는 것을 알게되어 염료를 생산하는 회사로 변경한 것이 BASF의 시작이었죠. 이후 탄산과 황산을 값싸고 질 좋게 생산하고, 1913년부터는 암모니아 생산을 독점해 사업을 확장해 나갑니다. 제 2차 세계대전 중에는 아우슈비츠에 공장을 만들어 전쟁 포로를 강제 노역시켰으며, 수용소의 죄수들을 죽이는 데 사용된 치클론-B를 생산하기도 한 전범 기업이기도 하죠. 전쟁 이후에는 플로스티렌, 스티로포르 등을 개발하며 사업을 이어갑니다.
•
이처럼 화학의 활용은 무기와 고분자 물질 생산을 통해 이루어집니다. 제약도 있긴 한데 제약은 또 너무 큰 이야기라 여기서는 맛만 보고 넘어가도록 하겠습니다.
Fig.1 화약이 만들어낸 이스라엘?!
① 노벨상의 시작
Figure.1 머스킷 총의 연기 ⓒwww.flickr.com/photos/wiblick/2201650911
나폴레옹 전쟁 이전까지의 총은 발사 후에 연기가 많이 발생해 시야를 확보하는 데 문제가 많았습니다. 게다가 무엇보다도 화약이 습기를 머금는 특성이 있었죠. 이를 해결하기 위해 화학자들은 화약을 연구합니다. 기존의 흑색 화약은 라부아지에Antoine-Laurent de Lavoisier 와 베르톨레Claude Louis Berthollet 에 의해 염소산 포타슘으로 발전했고, 이후 1846년 아스카니오 소브레로Ascanio Sobrero 가 나이트로글리세린을 만들어냅니다. 나이트로글리세린은 폭발력이 강한 물질이지만 열이나 압력에 민감해 쉽게 폭발하고, 폭발을 예측하기도 어려웠기 때문에 발명한 소브레로조차 사용을 반대했습니다. 기존의 흑색 화약에 비해 연기가 적고 효율이 뛰어난 무연 화약은 1889년경 프레드릭 아벨Frederick Augustus Abel 이 개발합니다.
Figure.2 노벨상의 그 노벨
한편 알프레드 베른하르드 노벨Alred Bermhartd Nobel 은 나이트로글리세린을 톱밥이나 규조토에 흡수시킨 형태로 열과 압력에 대한 안정성을 확보한 ‘다이너마이트’를 개발하는 데 성공합니다. 다이너마이트는 광산업 분야의 필수 장비가 되어 노벨은 막대한 부를 얻는데요. 잘 알려져 있다시피 노벨은 사망하기 1년 전 재산을 헌납한 후 물리학, 화학, 생리학 • 의학, 문학, 평화 분야에서 인류에 크게 공헌한 사람을 각각 선정해 상을 수여하라는 유언장을 남겨 노벨상이 탄생합니다.
② 화약이 만들어낸 이스라엘
Figure.3 아세톤 생산으로 이스라엘 대통령까지 된 바이츠만
아벨이 개발한 무연 화약은 영국군에 쓰였습니다. 이 무연 화약을 제조하는 데 아세톤이 필요했는데요. 문제는 제1차 세계대전까지만 해도 아세톤은 독일을 비롯한 중부 유럽 국가에 매장되어 있는 아세트산 칼륨에서 추출한다는 것이었죠. 제1차 세계대전에 적국이 된 독일은 당연히 영국에 아세트산 칼륨 수출을 막았습니다.
이 문제는 차임 바이츠만Chaim Azriel Weizmann 이 해결합니다. 바이츠만은 고무를 인공적으로 합성하는 방법을 찾기 위해 미생물을 연구하던 중 우연히 클로스트리디아라는 세균이 설탕이나 포도당을 아세톤으로 발효시킬 수 있다는 사실을 발견합니다. 이를 통해 영국은 전시에도 아세톤을 생산할 수 있게된 거죠. 아세톤 생산이 전쟁 승리에 큰 역할을 했기에 당시 영국 수상 로이드David Lloyd George 는 바이츠만에게 보답하려고 하는데요. 유대인이었던 바이츠만은 팔레스타인 지역에 유태인들의 독립국가를 건설하는 데 지원해 줄 것을 요청했고 1917년의 ‘밸푸어 선언’을 이끌어내게 됩니다. 1948년 이스라엘이 건국된 이후 바이츠만은 이스라일 초대 대통령이 되죠.
③ 비료의 무기의 한 끝차이
Figure.4 사람을 살리고 죽인 프리츠 하버
제 2차 세계대전 당시에는 영국군이 해상 무역을 봉쇄해 독일의 물자 수급을 막았는데요. 이 과정에서 독일의 하버Fritz Jakob Haber 가 공기 중의 질소를 인공적으로 농축해 암모니아로 합성하는 방법을 개발합니다. 이로서 비료와 화약의 원료를 공기 중에서 만들어낼 수 있게 된 것이었죠. 이후 이 공정은 독일기업이었던 BASF가 독점 생산합니다. 하버는 인류의 기근을 해결했다는 공로로 노벨 화학상을 수상하는데요. 하버의 노벨상 수상에 대해 항의가 많았습니다. 하버는 화학무기를 최초로 만들고 제안한 인물이었기 때문이죠. 1915년 4월 22일 프랑스 북부의 이프레 지역에 하버가 만든 염소 가스가 사용됩니다. 이를 대응하기 위해 연합군은 포스젠 가스로 반격하고, 독일군은 겨자 가스로 대응했죠.
Fig.2 보라색이 만든 아스피린
Figure.5 화학 염료 열풍을 그린 풍자 만화
19세기 중반 의약의 화두는 말라리아 치료제였습니다. 말라리아 치료제인 퀴닌은 남아메리카에서 자라는 키나나무 껍질에서만 얻을 수 있었기 때문에 수요만큼 공급이 따라주지 못했거든요. 이에 영국 왕립화학대학교에서는 아우구스트 빌헬름 폰 호프만Auguct Wilhein yoa Hotmamn 을 필두로 이 문제를 해결하고자 했죠. 호프만은 그의 조수였던 19세의 윌리엄 퍼킨Sir William Henry Perkin 에게 퀴닌을 화학적으로 합성해 보라는 연구 주제를 주었습니다.
Figure.6 1860년 퍼킨이 모베인으로 염색한 실크 ⓒHasselblad H4D
1853년 퍼킨은 퀴닌을 만들어내기 위한 실험하던 중에 새로운 발견을 하게 됩니다. 플라스크를 알코올로 씻던 중 선명한 보라색이 관찰된 것이었죠. 당시 보라색 염료는 천연 소라고둥에서 극소량만 추출할 수 있는 색상으로 고가의 염료였습니다. 그는 이 발견의 상업적 가치를 알아보고 실험실을 때려치우고 염료 사업을 시작합니다. 화학적으로 만들어낸 이 보라색 물질에 모베인이라는 이름을 붙여 판매했죠. 마침 모베인으로 염색한 천이 빅토리아 여왕의 눈에 띄게 되고 퍼킨은 대박이 납니다. 참고로 퍼킨의 지도 교수였던 호프만도 1861년 알데히드 그린이라는 염료를 만듭니다.
퍼킨의 성공을 본 프리드리히 엥겔호른Friedrich Engelhorn 은 염료 생산업에 뛰어들어 오늘날 글로벌 1위 화학회사인 BASF를 설립합니다. 1876년 BASF의 연구원 하인리히 카로Heinrich Caro 는 인디고와 메틸렌 블루라는 염료를 발명하는데요. 파울 에를리히는 메틸렌블루가 말라리아 유충을 선택적으로 염색한다는 사실을 밝혀냅니다. 그렇다면 ‘메틸렌 블루에 독성 물질을 붙이면 말라리아 유충을 선택적으로 죽이는 것도 가능하지 않을까?’ 하는 생각에 다다르죠. 메틸렌 블루를 만든 파울 에를리히는 이를 연구하고 결과적으로 말라리아가 아닌 매독 치료제인 살바르산을 개발합니다.
Figure.7 1899년 바이엘의 아스피린 ⓒBayer AG
퍼킨의 성공을 보고 설립한 또 다른 유명한 회사 중에 바이엘이 있습니다. 초기에는 마젠타 염료가 주요 제품이었지만 1897년 바이엘에 재직 중이었던 샤를 게르하르트Charles Frédéric Gerhardt 가 아스피린을 만들어낸 뒤 본격적으로 의약품에 집중합니다. 아스피린 이전에는 버드나무 껍질에서 추출한 살리실산을 해열, 진통제로 사용했었는데요. 위벽을 자극하는 부작용이 있던 살리실산을 보완해 화학적으로 만들어낸 것이 아스피린이었죠.
제 1차 세계대전에서 독일이 패배하자 많은 회사에서 바이엘과 아스피린 상표를 복제약에 마음대로 썼는데요. 1944년 아스피린 상표와 로고를 돌려받기까지 사람들의 인식에 '아스피린=바이엘'이라는 인식이 심어져서 오히려 성공했다는 의견도 있습니다.
Fig.3 현대의 연금술, 고분자 화학
① 고무가 타이어가 되기까지
Figure.8 원주민들이 고무공을 가지고 노는 것을 본 콜럼버스 ⓒart.com
고분자라는 개념은 20세기에 들어서야 정립됩니다. 그 이전에는 고분자가 무엇인지도 모른 채 사람들은 자연에서 얻어지는 고분자 물질을 사용했죠. 대표적인 예로 고무가 있습니다. 서인도제도 원주민들은 사람들은 고무나무 수액에서 얻은 천연고무로 공, 샌들과 같은 제품을 만들어 사용했는데요. 콜럼버스가 이를 유럽에 전파하면서 널리 쓰였죠.
Figure.9 찰스 매킨토시의 맥코트 ⓒmackintosh.com
산소를 발견하고, 탄산수를 발명하기도 했던 프리스틀리는 고무로 연필 필기를 지울 수 있다는 사실을 발견하고 지우개를 만들어내기도 합니다. 또한 1824년 찰스 매킨토시Charles Macintosh 는 천연고무를 녹여 옷감에 펴 바르는 방식으로 최초의 방수 우비를 발명합니다. 이 우비는 매킨토시 코트라 불리는 데, 오늘날 맥코트의 탄생이었죠.
Figure.10 찰스 굿이어 ⓒcorporate.goodyear.com
하지만 생고무는 날씨가 더우면 냄새가 나고 끈적끈적하게 녹아버리고 추우면 딱딱하게 굳어버리는 문제가 있었습니다. 이를 해결한 것이 찰스 굿이어Charles Goodyear 이죠. 평생 고무를 연구했던 굿이어는 1839년 경에 실수로 고무와 황을 섞어둔 그릇을 난로에 떨어트리고 맙니다. 그런데 고무가 녹지 않고 살짝 그을리기만 했죠. 즉 고무에 황을 첨가하면 고무의 내구성을 높일 수 있다는 것을 발견한 것이었습니다. 굿이어는 이를 가지고 고무콘돔을 만들기도 하는 등 사업을 시도합니다. 하지만 굿이어는 연구비와 특허침해소송으로 죽을 때까지 20만 달러의 빚이 있었다고 하죠. 반세기 후 미국의 사업가 프랭크 세이버링Frank Seiberling 이 그의 이름을 기려 굿이어타이어앤드러버 컴퍼니를 설립하면서 굿이어는 타이어의 대명사가 됩니다.
② 당구붐이 만들어낸 플라스틱
Figure.11 1859년 미국에 있는 마이클 펠런의 당구 살롱
고분자 물질의 대표주자는 바로 플라스틱입니다. 잘 알려져 있다시피 플라스틱의 시작에는 코끼리와 관련이 있습니다. 19세기 중반 코끼리 상아는 피아노 건반, 장신구, 무엇보다도 당구공에 쓰이면서 코끼리 밀렵 문제가 심각했는데요. 이에 1863년 당구 선수 마이클 펠런Michael Phelan 이 상아를 대체해 당구공을 만들 수 있는 신소재 개발하는 자에게 1만 달러를 주겠다는 신문광고를 냅니다. 이 광고를 본 뉴욕의 존 웨슬리 하야트John Wesley Hyatt 가 신소재 개발에 뛰어들죠. 1855년 알렉산더 파크Alexander Parkes 가 면화에 질산을 넣어서 만든 파케신이라는 물질이 있었는데요. 1869년 하야트는 여기에 유기용제를 섞어 개량해 잘 늘어나면서 단단하게 만들 수 있는 하얀색의 물질, 셀룰로이드를 만들어냈죠. 셀룰로이드는 상아와 같은 무늬와 색을 낼 수 있었습니다.
하지만 하야트는 상금을 받지는 못했습니다. 셀룰로이드가 상아와 같은 탄성을 가지지 못했고, 더 큰 문제는 하야트가 만든 당구공은 세게 부딪히면서 폭발하는 문제가 있었거든요. 대신 하야트의 셀룰로이드는 당시 아주 비쌌던 상아 빗을 대체하게 됩니다.
이후 베이클랜드Leo Hendrik Baekeland 가 페놀과 포름알데히드를 반응시켜 베이클라이트라는 플라스틱을 만들면서 해결됩니다. 셀룰로이드와 다르게 베이클라이트는 물성도 좋고 안정성이 매우 뛰어나 다양한 산업 분야에 적용되었죠. 진정한 플라스틱이 탄생하게 된 순간이었죠.
오늘날 플라스틱하면 가장 먼저 떠오르는 것은 페트병이지 않을까 싶은데요. 페트병은 의외로 등장한 지 얼마 되지 않았습니다. 당시의 플라스틱으로 탄산음료를 담으면 폭발했거든요. 너세니얼 와이어스Nathaniel Wyeth 은 10년간 페트병 연구 끝에 플라스틱은 약한 물체지만 플라스틱을 구성하는 긴 가닥의 분자들이 서로 얽히면 강력해진다는 사실을 밝혀냅니다. 1973년 플라스틱에 나일론 원사를 결합해 패트병을 만드는 방법을 개발하죠. 페트병은 개발 직후 탄산음료 산업의 호황으로 바로 사용되었죠.
③ 고분자 원리의 발견
이렇듯 실험을 통해 새로운 고분자 물질들이 발견되고 있었지만, 화학자들은 그 구조와 생성 원리가 어떻게 되는지는 알지 못했습니다. 사실 20세기 초까지 화학자들은 화합물이 수만 이상의 분자량을 가지는 거대한 형태로 결합되어 있다는 점을 납득하지 못했습니다. 고분자는 겉보기에만 크게 보이고 사실은 작은 물질들이 서로 뭉쳐져 있는 것으로 생각했죠. 그럴 수밖에 없었던게 당시 알려진 무거운 금속 화합물도 분자량이 500~600이었던 반면 고분자 물질은 1만~30만에 달했거든요.
Figure.12 고분자 물질의 구조를 밝힌 슈타우딩거, 1953년 노벨 화학상을 받았다 ⓒFr. Schmelhaus / ETH Zürich
1920년 독일의 화학자 헤르만 슈타우딩거Hermann Staudinger 는 <중합에 대하여>라는 논문에서 고분자물질이 작은 물질들이 단순히 뭉쳐져 있는 것이 아니라 직접적인 결합을 통해 단단히 결합되어 있으며 반복성을 가지는 거대한 사슬이라고 주장합니다. 이후 점성 비교, 분광학적 기법 등을 통해 슈타우딩거의 내용이 증명되죠. 더 나아가서 허먼 프랜시스 마크Heman Francis Mark 가 X-선 회절을 이용해 고분자물질이 슈타우딩거가 상상한 것처럼 단단하게 결합되어 있는 것이 아니라 회전할 수 있는 사슬 형태의 느슨한 구조라는 것을 밝혀냅니다.
④ 나일론
Figure.13 캐러더스의 모습
19세기 화약 회사로 성장한 듀폰 사는 1920년대부터 재료 과학에 투자합니다. 그 과정에서 윌리스 캐러더스Wallace Hume Carothers 를 고용합니다. 캐러더스는 고분자 섬유 연구에 전념했는데요. 캐러더스 연구팀의 줄리언 힐Juian W.H. 이 비커 바닥에 끈적끈적하게 눌어붙은 폴리에스테르를 유리 막대에 묻혀 끌어당기자, 실처럼 길게 늘어나는 현상을 발견합니다. 이를 보고 고분자 물질을 실 형태로 뽑아낼 수 있겠다는 아이디어를 얻습니다. 곧이어 폴리에스테르를 실 형태로 뽑아내는 데 성공했고, 이는 인공 실크로 발전하게 됩니다. 하지만 폴리에스테르는 열을 가하면 형태를 유지하지 못하고, 물리적 내구성도 너무 약하며 심지어는 물에 녹는 문제가 있었죠. 1935년 이 문제를 해결한 물질인 ‘6-6 나일론’이 탄생합니다.
Figure.14 1938년 나일론을 대중에게 선보이는 모습 ⓒsciencehistory.org
듀폰 사는 개발한 물질을 나일론이라 이름붙여 1938년 세계박람회에서 공개하고 이듬해 실크 스타킹을 대체하는 나일론 스타킹을 판매합니다. 첫 해에는 미국 델라웨어 주 월밍턴에 사는 사람들을 대상으로만 인당 세 켤레를 살 수 있도록 했는데, 세계 각국의 수천 명의 여성이 주소를 얻기 위해 월밍턴의 호텔에 투숙하는 일이 벌어졌죠.
당시 세계 스타킹 시장은 일본산 실크가 점령하고 있었습니다. 그런데 나일론 스타킹이 등장하자 일본산 실크 스타킹 산업은 크게 흔들리게 되죠. 이에 일본에서는 나일론에 대한 음모론이 등장하는데요. Nylon을 반대로 읽으면 농림성 발음과 유사하다는 주장, Nylon은 ‘Now You Lousy Old Nipponese!’의 첫 글자를 따온 것이라는 주장 등이었죠. 어찌되었든 나일론은 실크 스타킹을 대체했고, 칫솔의 솔, 나일론 줄, 나일론 플라스틱, 낙하산 등 다양한 제품에 쓰였습니다.
⑤ 테팔의 탄생
Figure.15 테팔 후라이팬 초기 모습 ⓒTefal
듀폰 사가 발명한 유명한 물질 중에는 폴리테트라플루오로에틸렌 일명 테플론도 있습니다. 테플론은 1938년 로이 조지프 플런켓Rory Joseph Plunket 에 의해 발견됩니다. 플런켓은 플루오린화 탄화수소를 담아 둔 가스 실린더의 밸브를 열었는데 아무것도 배출되지 않았죠. 이상하게 여긴 플런켓은 가스 실린더를 잘라 내부를 관찰했는데, 흰색 가루가 덩어리져 가스 실린더 내부를 뒤덮고 있었습니다. 이 물질을 실험해 보았더니 인체에 무해하며 강한 산이나 염기, 고온에도, 그리고 물이나 유기 용매에도 전혀 녹지 않는 경이로운 내구성을 보였으며 미끈거리는 물성을 가지고 있었습니다. 테플론은 이후 원자폭탄 프로젝트에서 파이프와 밸브의 부식을 방지하기 위한 코팅 용도로 쓰였습니다.
테플론은 1946년부터 시중에 팔렸는데요. 프랑스의 기술자 마르크 그레과르Marc Grégoire 가 테플론을 가져다 낚싯줄에 코팅해보면 어떨까 하고 연구하고 있었죠. 그러던 중 아내가 자꾸 눌어붙는 무쇠 프라이팬에 대한 불만을 이야기하던 것에 영감을 얻어 프라이팬에 코팅해보았고, 뛰어난 성능을 보이자 1954년 듀폰으로부터 판권을 구매해 판매하기 시작했죠. 그레과르가 세운 회사가 테플론과 알루미늄을 합친 테팔Tefal 입니다.
Reference.
•
백승만. (2023). 분자 조각가들. 해나무
•
장홍제. (2021). 화학연대기. EBSBOOKS
•
정진호. (2017). 위대하고 위험한 약 이야기 : 질병과 맞서 싸워온 인류의 열망과 과학. 푸른숲
•
홍수열. (2020). 그건 쓰레기가 아니라고요. 슬로비
•
이종호. (2014). [기술이 바꾼 미래] 윌리엄 헨리 퍼킨 : 합성 염료 시대를 열다. 동아사이언스. URL : https://www.dongascience.com/special.php?idx=635
•
진정일. (2022). [월간화학] 나일론의 탄생. 한화토탈에너지스 케미인 공식 블로그. URL : https://www.chemi-in.com/728
•
최성우. (2018). 고무에 미친 인간 ‘굿이어’. 사이언스타임즈. URL : https://www.sciencetimes.co.kr/news/고무에-미친-인간-굿이어/